由中山大学肿瘤防治中心黄欣教授牵头的一项安罗替尼联合TQB2450(新型PD-L1抑制剂)治疗铂耐药或难治性卵巢癌(ACTION)的临床研究,本研究的初步报道既往在美国临床肿瘤学会(ASCO)公布,此次研究最终结果于2022年7月20日荣登国际权威期刊Cell Reports Medicine(IF=16.988),该研究中安罗替尼联合TQB2450治疗展现出良好抗肿瘤活性,结果值得肯定。这是继今年安罗替尼联合免疫在宫颈癌和子宫内膜癌两篇文章在国际权威期刊发表后,安罗替尼在妇瘤领域的又一次实力绽放。本文将对研究成果进行详细解读。 卵巢癌在全球女性癌症相关死亡率排名居第八位,70%的患者确诊时已是晚期[1]。尽管一线含铂化疗较为有效,但大多数患者在2年内会复发[2]。几乎所有的患者最终都会对铂类药物产生耐药性[3]。使用单药非铂类药物被认为是铂耐药复发的标准治疗[4]。然而,单药治疗的客观缓解率(ORR)较低约10%-20%,无进展间期较短约3-4月[4-6]。 免疫检查点抑制剂(ICI)治疗改变了多种癌症的治疗格局[7-9]。尽管既往研究数据显示卵巢癌是一种免疫原性疾病[10],但卵巢癌患者对PD-1/ PD-L1抑制剂的应答率似乎较低,ORR在10%左右[11]。PD-1/PD-L1抑制剂联合抗血管生成治疗被认为可增强单药治疗的疗效,既往两项PD-1/PD-L1抑制剂联合抗血管生成药物的研究显示在复发性卵巢癌患者中的前景[11-13]。然而目前,PD-1/PD-L1抑制剂与小分子多靶点TKI联合治疗的疗效知之甚少。安罗替尼是一种新型小分子TKI,对VEGFR、PDGFR、FGFR、c-Kit等靶点有着良好的抑制效果,具有抗肿瘤血管生成和抑制肿瘤生长的双重功效。在一项正在进行的安罗替尼单药治疗铂耐药或铂难治性卵巢癌患者的Ⅱ期研究中,初步结果显示ORR为14.3%,疾病控制率(DCR)为71.4%[14]。TQB2450 是一种抗PD-L1的人源化IgG1单克隆抗体,已在黑色素瘤和结肠癌小鼠模型中证明了抗肿瘤活性[15]。在临床前数据的支持下,TQB2450联合或不联合安罗替尼治疗晚期难治性胆道癌、三阴性乳腺癌、非小细胞肺癌和妇科肿瘤患者的临床试验正在进行中[16-18]。在此,我们介绍安罗替尼联合TQB2450治疗铂耐药或铂难治性卵巢癌患者的疗效和安全性。 入排标准:1.年龄18-70岁;2. 组织学确诊的铂耐药或铂难治的上皮性卵巢癌、输卵管癌和原发腹膜癌;3. ECOG评分0-1;4. 有客观可测量的病灶(RECIST 1.1)。患者的基线特征见表1。 试验设计:患者接受TQB2450 1200 mg静脉给药(第1天,每3周1次)。接受安罗替尼12 mg口服给药(每日1次,第1-14天,21天为一周期)。治疗持续至疾病进展(PD)、治疗不耐受或死亡、患者退出或退出研究。根据药物相关毒性和潜在临床获益,由研究者酌情调整安罗替尼剂量,最多允许减量两次,首次减量至10 mg每日一次,额外减量至8 mg每日一次。不允许进行TQB2450剂量调整。 研究终点:主要终点为ORR。次要终点包括无进展生存期(PFS)、总生存期(OS)、疾病控制率(DCR)、应答持续时间(DOR)和安全性(见图1)。 图1.研究设计 疗效显著:ORR为47.1%,中位PFS为7.8个月 2020年2月27日至2021年2月26日期间,共筛选了44例患者,其中34例患者符合入组并接受研究方案治疗(全分析集和安全性集)。在符合方案集 (PPS) 中排除了1例 (2.9%) 由于在首次基线后肿瘤评估前因不良事件 (AE) 而中止治疗的患者(图 2)。 图2.患者分布 截至数据截止日期(2021年05月31日),中位随访时间为8.6个月(范围:2.3-15.3)。34例患者中的13例 (38.2%) 仍在接受治疗。21例 (61.8%) 患者中止治疗,其中16例因疾病进展 (47.1%),2例因AE(5.9%) 和3例因患者拒绝 (8.8%)。 在入组的前9例患者中,5例患者中观察到证实的缓解,达到了Simon两阶段第一阶段的 ORR阈值,试验继续完成招募。在全分析集中,34例患者中的16例达到部分缓解 (PR),ORR为47.1%(95% CI 29.8-64.9)(表2),另外3例患者为未证实的PR。在符合方案集中记录了相似的结果(表2)。34例患者中的17例(50.0%)达到疾病稳定(SD),因此DCR 为97.1%(95% CI 84.7-99.9;表2)。如图3A所示,33例可评价肿瘤评估患者中的26例 (78.8%) 出现一定程度的肿瘤缩小。 表2.根据RECIST 1.1评估的抗肿瘤活性 在16例确认客观缓解的患者中,中位起效时间为2.7个月(范围:1.3-7.0),未达到中位DOR(95% CI 5.3-未达到;图4A)。在61.3%(95% CI 25.1-84.0)患者中观察到DOR至少为8个月。图3B显示了所有患者接受治疗时间的游泳图。 图3.患者瀑布图和游泳图 截至数据截止日期,34例患者中的17例(50.0%)发生疾病进展。中位PFS为7.8个月(95% CI 4.9-未达到;图4B)。6个月PFS率为66.7%(95% CI 46.7-80.7),9个月PFS率为38.1%(95% CI 19.1–57.0),9例(26.5%)患者死亡。未达到中位总生存期 (OS)(95% CI 11.3-未达到;图4C)。 图4.患者的DOR、PFS和OS 所有34例患者 (100.0%) 均发生了任何级别的治疗相关不良事件(TRAEs)(表3):高血压 (n=31,91.2%)、掌跖红肿疼痛综合征 (n=25,73.5%)、高甘油三酯血症 (n=20,58.8%) 和甲状腺功能减退症(n=17,50.0%;表3)。24例(70.6%)患者发生3-4级TRAEs:最常见的是高血压 (n=10,29.4%)、掌跖红肿疼痛综合征 (n=10,29.4%)、高甘油三酯血症 (n=5,14.7%)、疲乏 (n=3,8.8%) 和体重减轻(n=3,8.8%)。未发生治疗相关的死亡事件。在34例患者中的5例(14.7%)观察到严重TRAEs,包括高血压、疲乏、肺炎和关节炎各1例(2.9%),以及天冬氨酸转氨酶和丙氨酸转氨酶升高1例 (2.9%)。 34例患者均接受至少一个完整周期的安罗替尼治疗。22例(64.7%)患者因为AEs中断安罗替尼给药。16例 (47.1%) 患者需要降低安罗替尼剂量,其中12例 (81.3%) 仅需要降低1次剂量,3例 (18.8%) 需要降低2次剂量。导致安罗替尼减量的最常见AE是掌跖红肿疼痛综合征 (10/16,62.5%)。34例患者中的8例(23.5%)发生TQB2450给药中断。8例(23.5%)患者需要皮质类固醇:2例肺炎;2例关节炎;皮疹、肌炎和甲状腺功能亢进各1例;1例天冬氨酸转氨酶和丙氨酸转氨酶升高。在接受皮质类固醇的患者中,1例患者中断TQB2450给药,1例患者永久停用TQB2450。2例(5.9%)患者因毒性退出研究:1例出现疲乏,1例出现4级天门冬氨酸氨基转移酶和丙氨酸氨基转移酶升高。 表3.安全性 22例患者进行了PD-L1表达检测,其中8例患者为PD-L1阳性,14例患者为PD-L1阴性。PD-L1阳性肿瘤患者的ORR为25.0%(95% CI,3.1%-65.1%),而PD-L1阴性肿瘤患者的ORR为92.9%(95% CI,66.1%-99.8%)(P=0.002)。PD-L1阳性患者的中位PFS为8.5个月(95% CI 2.6-未达到),PD-L1阴性患者中位PFS未达到(95% CI 6.8-未达到)(图5)。PD-L1阳性或PD-L1阴性患者之间的PFS差异无统计学显著性(P=0.28,图5)。 图5.根据PD-L1表达统计的中位PFS 本研究是安罗替尼联合免疫药物在卵巢癌领域的前瞻性研究,在这项研究中,安罗替尼联合TQB2450在铂耐药或铂难治性卵巢癌患者中表现出有前景的抗肿瘤活性,具有持久的缓解和可耐受的毒性。ORR为45.8%,中位PFS为7.8个月,中位OS未达到。一项Ⅲ期多中心随机试验(NCT05145218)安罗替尼联合TQB2450治疗铂耐药或铂难治性卵巢癌患者的研究正在进行中[19]。 安罗替尼作为正大天晴自主研发的抗肿瘤1.1类新药,自问世以来屡获殊荣。在非小细胞肺癌、小细胞肺癌、软组织肉瘤、甲状腺癌、食管鳞癌、结直肠癌、肝癌、肾癌、乳腺癌、宫颈癌、子宫内膜癌等中均有卓越表现,得到了国内外专家的一致认可。此项由我国学者引领的研究无疑为卵巢癌患者带来福音,未来也将在国际舞台上展现中国智慧。 为民族,抗肿瘤,正大天晴一直在行动! 专家简历 黄欣 教授 中山大学附属肿瘤医院 肿瘤妇科 主任医师 从事妇科肿瘤的医教研工作30余年。擅长各种妇科肿瘤的诊治工作,在妇科恶性肿瘤的手术治疗方面积累丰富经验,包括各种疑难复杂病例的手术治疗以及肿瘤复发后的大型手术,擅长手术,化疗和免疫靶向综合治疗妇科恶性肿瘤; 深入开展复发卵巢癌和宫颈癌的临床与基础研究,国内外率先提出并证明化疗加靶向“全口服”方案治疗铂耐药卵巢癌临床价值;率先采用 “免疫联合抗血管生成”治疗复发宫颈癌获得成功; 主持安罗替尼联合TQB2450治疗复发难治性铂耐药卵巢癌全国多中心前瞻性III期临床研究,主持多个多中心免疫靶向、免疫化疗联合手段治疗复发难治宫颈癌和卵巢癌的临床研究; 以第一/通讯作者在Lancet Oncology, Journal of Clinical Oncology,Gynecologic Oncology,等国际知名 SCI杂志 发表论文10多篇,累计影响因子>100。 蓝春燕 教授 中山大学附属肿瘤医院 妇科 主任医师 博士 硕士生导师 从事妇科肿瘤诊治工作10余年,擅长妇科恶性肿瘤的根治性手术,擅长妇科肿瘤(宫颈癌、卵巢癌、子宫内膜癌等)的靶向治疗、免疫治疗等综合治疗。 其团队提出采用化疗+抗血管生成的“双口服”方案治疗铂耐药卵巢癌,研究结果发表于国际著名肿瘤学杂志Lancet oncol。 其团队率先报道了“免疫+抗血管生成”治疗模式在复发性宫颈癌的抗肿瘤疗效,研究结果发表于国际著名肿瘤学杂志J Clin Oncol。 主持多项宫颈癌、卵巢癌的抗癌新药临床试验,助推妇科肿瘤靶向、免疫新药的研发。 以第一负责人主持国家自然科学基金、广东省自然科学基金面上项目等多项课题。 广东省杰出青年医学人才 参考文献: [1] Sung, H., Ferlay, J., Siegel, R. L., Laversanne, M., Soerjomataram, I., Jemal, A., and Bray, F. (2021). Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J. Clin. 71, 209-249. [2] Ozols, R. F., Bundy, B. N., Greer, B. E., Fowler, J. M., Clarke-Pearson, D., Burger, R. A., Mannel, R. S., DeGeest, K., Hartenbach, E. M., Baergen, R., and Gynecologic Oncology, G. (2003). Phase III trial of carboplatin and paclitaxel compared with cisplatin and paclitaxel in patients with optimally resected stage III ovarian cancer: a Gynecologic Oncology Group study. J. Clin. Oncol. 21, 3194-3200. [3] International Collaborative Ovarian Neoplasm, G. (2002). Paclitaxel plus carboplatin versus standard chemotherapy with either single-agent carboplatin or cyclophosphamide, doxorubicin, and cisplatin in women with ovarian cancer: the ICON3 randomised trial. Lancet 360, 505-515. [4] Pujade-Lauraine, E., Banerjee, S., and Pignata, S. (2019). Management of Platinum-Resistant, Relapsed Epithelial Ovarian Cancer and New Drug Perspectives. J. Clin. Oncol. 37, 2437-2448. [5] Gynecologic Oncology, G., Markman, M., Blessing, J., Rubin, S. C., Connor, J., Hanjani, P., and Waggoner, S. (2006). Phase II trial of weekly paclitaxel (80 mg/m2) in platinum and paclitaxel-resistant ovarian and primary peritoneal cancers: a Gynecologic Oncology Group study. Gynecol. Oncol. 101, 436-440. [6] Mutch, D. G., Orlando, M., Goss, T., Teneriello, M. G., Gordon, A. N., McMeekin, S. D., Wang, Y., Scribner, D. R., Jr., Marciniack, M., Naumann, R. W., and Secord, A. A. (2007). Randomized phase III trial of gemcitabine compared with pegylated liposomal doxorubicin in patients with platinum-resistant ovarian cancer. J. Clin. Oncol. 25, 2811-2818. [7] Hodi, F. S., O'Day, S. J., McDermott, D. F., Weber, R. W., Sosman, J. A., Haanen, J. B., Gonzalez, R., Robert, C., Schadendorf, D., Hassel, J. C., et al. (2010). Improved survival with Ipilimumab in patients with metastatic melanoma. N. Engl. J. Med. 363, 711-723. [8] Brahmer, J., Reckamp, K. L., Baas, P., Crino, L., Eberhardt, W. E., Poddubskaya, E., Antonia, S., Pluzanski, A., Vokes, E. E., Holgado, E., et al. (2015). nivolumab versus Docetaxel in Advanced Squamous-Cell Non-Small-Cell Lung Cancer. N. Engl. J. Med. 373, 123-135. [9] Reck, M., Rodriguez-Abreu, D., Robinson, A. G., Hui, R., Csoszi, T., Fulop, A., Gottfried, M., Peled, N., Tafreshi, A., Cuffe, S., et al. (2016). pembrolizumab versus Chemotherapy for PD-L1-Positive Non-Small-Cell Lung Cancer. N. Engl. J. Med. 375, 1823-1833. [10] Zhang, L., Conejo-Garcia, J. R., Katsaros, D., Gimotty, P. A., Massobrio, M., Regnani, G., Makrigiannakis, A., Gray, H., Schlienger, K., Liebman, M. N., et al. (2003). Intratumoral T cells, recurrence, and survival in epithelial ovarian cancer. N. Engl. J. Med. 348, 203-213. [11] Hamanishi, J., Mandai, M., Ikeda, T., Minami, M., Kawaguchi, A., Murayama, T., Kanai, M., Mori, Y., Matsumoto, S., Chikuma, S., et al. (2015). Safety and Antitumor Activity of Anti-PD-1 Antibody, nivolumab, in Patients With Platinum-Resistant Ovarian Cancer. J Clin Oncol 33, 4015-4022. [12] Matulonis, U. A., Shapira-Frommer, R., Santin, A. D., Lisyanskaya, A. S., Pignata, S., Vergote, I., RASpagliesi, F., Sonke, G. S., Birrer, M., Provencher, D. M., et al. (2019). Antitumor activity and safety of pembrolizumab in patients with advanced recurrent ovarian cancer: results from the phase II KEYNOTE-100 study. Ann. Oncol. 30, 1080-1087. [13] Disis, M. L., Taylor, M. H., Kelly, K., Beck, J. T., Gordon, M., Moore, K. M., Patel, M. R., Chaves, J., Park, H., Mita, A. C., et al. (2019). Efficacy and Safety of avelumab for Patients With Recurrent or Refractory Ovarian Cancer: Phase 1b Results From the JAVELIN Solid Tumor Trial. JAMA Oncol. 5, 393-401. [14] Shan, B., Wang, S., Wang, H. (2020). Anlotinib in patients with recurrent platinum resistant or refractory ovarian carcinoma: A prospective, single-arm, single-center, phase II clinical study. (Abstract 6061). J. Clin. Oncol. 38, Issue 15_suppl. [15] Wei, Z., Yang, L., Li, Y., Lu, J., Zhang, X., Tian, X., Zha, J., Sun, Z., Qiu, J., Wang, Z., Reddy, M., Choy, G. and Redkar, S. (2018). CBT-502 (TQB2450), a novel anti-PD-L1 antibody, demonstrates favorable activity in MC-38/H-11 murine colon and A375 human melanoma animal models. (Abstract A200). Molecular Cancer Therapeutics. [16] Zhou, J., Gong, J., Cao Y., Peng, Z., Yuan, J., Wang, X., Lu, M., Shen, L. (2021). Anlotinib plus TQB2450 in patients with advanced refractory biliary tract cancer (BTC): An open-label, dose-escalating, and dose-expansion cohort of phase Ib trial. (Gastrointestinal Cancers Symposium, Abstract 292). J. Clin. Oncol. 39, Issue 3_suppl. [17] Wang, J., Xu, B., Sun, T., Ouyang, Q., Han, Y., Li, Q., Zhang, P., Ma, F., Luo, Y., Fan, Y., Cai, R., Li, Q., Lan, B., Mo, H., Wang, J., Li, Y. (2021). A phase Ib study of TQB2450 plus anlotinib in patients with advanced triple-negative breast cancer. (Abstract 1074). J. Clin. Oncol. 39, Issue 15_suppl. [18] Cheng, Y., Cui, H., Wu, C., Wang, Y., Zhang, T., Xin, Y., Xu, J., Chen, Y., Li, Z., Wang, Y., Wei, H., Zhu, J., Du, T. (2020). A phase Ib study of TQ-B2450 plus anlotinib in patients with advanced solid tumor. (Abstract 3065). J. Clin. Oncol. 38, Issue 15_suppl. [19]Chun-Yan Lan, Jing Zhao, Fan Yang, Ying Xiong, Rong Li, Yu Huang, Jing Wang, Chang Liu, Xue-Han Bi, Hai-Hong Jin, Jin Meng, Wei-Hong Zhao, Li Zhang, Ya-Fei Wang, Min Zheng, Xin Huang, Anlotinib combined with TQB2450 in patients with platinum-resistant or -refractory ovarian cancer: A multi-center, single-arm, phase 1b trial,Cell Reports Medicine,Volume 3, Issue 7, 2022, 100689.
研究背景
评估安罗替尼联合免疫药物在卵巢癌的有效性和安全性的前瞻性研究
 表1.患者的基线特征
表1.患者的基线特征
安罗替尼联合TQB2450为铂耐药或铂难治性卵巢癌提供治疗的新选择




安全性可控

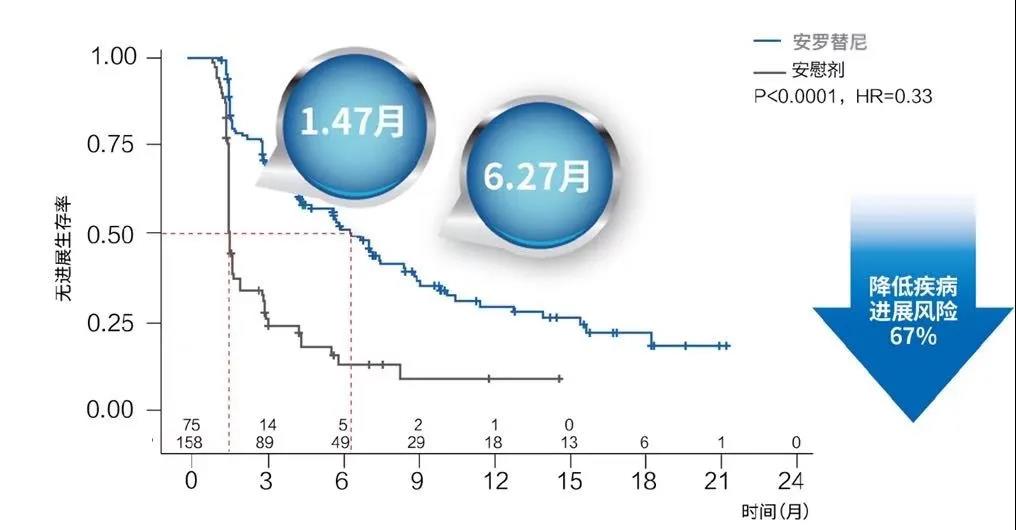
生物标记物探索:PD-L1表达

结论
展望